鄭州源創基因科技有限公司成立于2016年,由哥倫比亞大學博士后趙輝,歸國創辦的國家高新技術企業。擁有97項知識產權及實用技術,業務遍布上海、重慶、深圳、北京等城市,總部在鄭州航空港區。
糖尿病是一種常見的代謝性疾病,全球患者人數已超過4億。而最新研究發現,NK細胞外泌體或許能為糖尿病的治療帶來新的曙光。

NK細胞外泌體
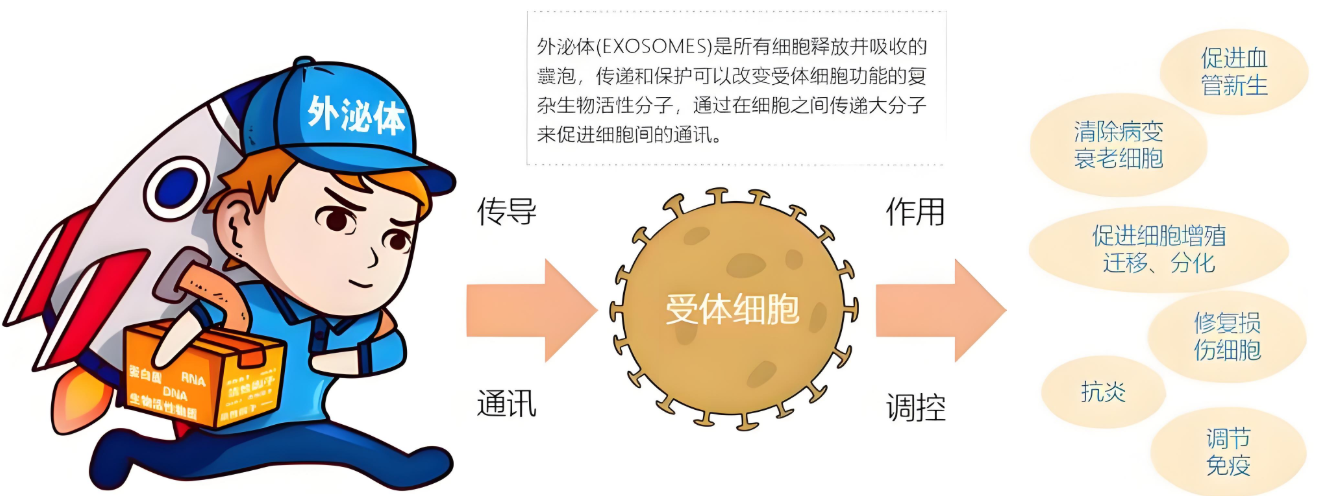
NK細胞(自然殺傷細胞)是免疫系統的重要組成部分,能夠通過調節炎癥反應影響機體代謝。外泌體是細胞分泌的納米級囊泡(直徑約30–150納米),可攜帶蛋白質、RNA等生物活性分子,在細胞間充當“信使”角色。
然而,NK細胞如何通過外泌體調控胰島素敏感性,一直是科學界尚未解開的謎題。
近期,中國藥科大學研究團隊在《Signal Transduction and Targeted Therapy》上發表論文,首次揭示:來自瘦鼠NK細胞的外泌體,可通過特定微小RNA(如miR-1249-3p)改善胰島素抵抗和炎癥反應,為2型糖尿病的治療提供了新的分子靶點。

NK細胞外泌體改善胰島素抵抗的作用機制
抑制炎癥反應
研究發現,NK細胞外泌體能夠顯著降低內臟脂肪和肝臟中炎癥因子(如IL-6、TNF-α)的水平,而這些因子正是導致胰島素抵抗的重要因素。通過抑制炎癥反應,外泌體有助于恢復組織對胰島素的敏感性。
促進代謝調節
NK細胞外泌體攜帶的miR-1249-3p等微小RNA,可激活胰島素信號通路中的關鍵分子(如p-Akt、PPARγ和GLUT4),促使細胞恢復對胰島素的響應,從而提升血糖的吸收和利用效率。
精準靶向作用
實驗顯示,這些外泌體主要富集于小鼠的內臟脂肪和肝臟——糖尿病代謝紊亂最突出的區域。這種組織特異性使外泌體能夠精準作用于代謝異常部位,發揮治療效果。
NK細胞外泌體改善胰島素抵抗的實驗證據
動物實驗
研究人員構建了2型糖尿病小鼠模型(通過高脂飲食和低劑量鏈脲佐菌素誘導),并從瘦鼠和胖鼠的脾臟NK細胞中分離外泌體,注射至糖尿病小鼠體內。
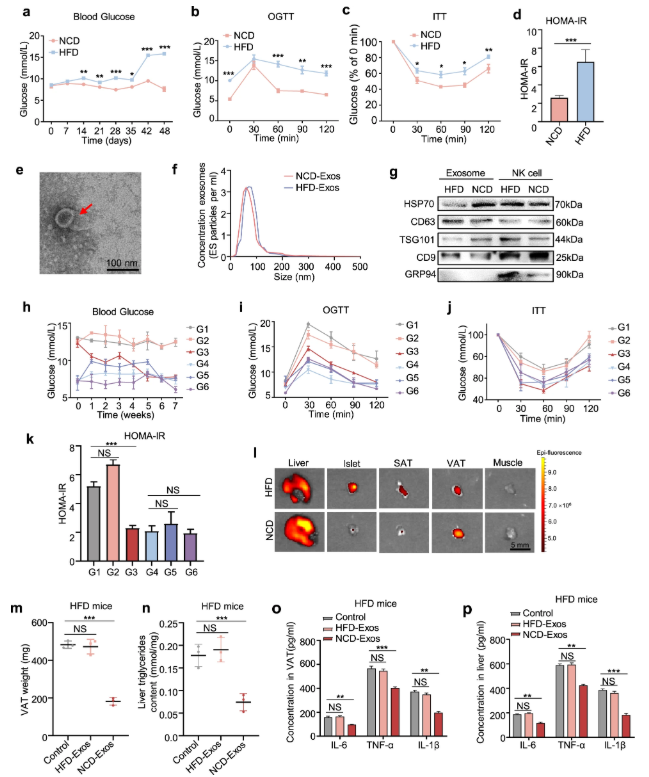
結果顯示,接受瘦鼠外泌體的小鼠體重逐漸恢復,空腹血糖顯著下降,口服葡萄糖耐量(OGTT)和胰島素耐量(ITT)結果改善,胰島素抵抗指數(HOMA-IR)也明顯降低。進一步分析發現,外泌體主要聚集在內臟脂肪和肝臟中,不僅減輕了脂肪重量和肝內甘油沉積,還降低了IL-6、TNF-α等炎癥因子水平,并增強了胰島素信號通路活性。而胖鼠來源的外泌體則未見明顯效果。
體外實驗
在3T3-L1脂肪細胞和AML12肝細胞中進行的實驗進一步驗證:瘦鼠外泌體可促進脂肪細胞攝取葡萄糖,抑制肝細胞生成葡萄糖,并減少炎癥因子分泌。同樣,胖鼠外泌體未表現出上述作用。

關鍵作用因子是什么?
基因芯片分析顯示,瘦鼠外泌體中miR-1249-3p的含量顯著高于胖鼠。進一步實驗證實,該微小RNA可通過外泌體從NK細胞傳遞至脂肪細胞和肝細胞。研究人員還觀察到,在細胞中轉入miR-1249-3p模擬物可重現外泌體的改善效果,而使用抑制劑阻斷miR-1249-3p后,外泌體的作用即消失。這表明miR-1249-3p是外泌體改善胰島素抵抗的核心成分。
臨床應用前景
該研究不僅首次揭示NK細胞可通過外泌體遠距離調控代謝,還明確了miR-1249-3p–SKOR1–SMAD6–TLR4/NF-κB這一全新信號軸,為2型糖尿病的治療提供了多個潛在靶點。未來,無論是補充miR-1249-3p,或是抑制SKOR1,均可能成為新的治療策略。
當然,該研究仍處于起步階段。目前所有結果均來自小鼠實驗,后續需在人體中驗證miR-1249-3p的功能。此外,如何實現外泌體的大規模臨床級制備與精準遞送,也是未來需要解決的關鍵問題。盡管如此,這一來自瘦鼠NK細胞外泌體的“微小英雄”,無疑為糖尿病治療照亮了新的道路。
結語
NK細胞外泌體的研究為糖尿病治療提供了全新視角。從改善胰島素抵抗到調控炎癥反應,從動物實驗到未來可能的臨床轉化,這些微小囊泡展現出巨大的潛力。隨著研究的深入與技術的發展,我們有理由期待,基于NK細胞外泌體的療法將為糖尿病患者帶來新的希望。
資料來源:再生外泌體
https://www.nature.com/articles/s41392-021-00805-y
https://mp.weixin.qq.com/s/bI4mWsAYS-dnmtI3f2BiDA